Christian Barillot : ce que pourraient voir les chirurgiens pendant une intervention

Directeur de recherche au CNRS, Christian Barillot s’est intéressé au traitement de l’information, du signal et de l’image dès ses travaux de doctorat. Il approfondit ce thème aux États-Unis, où il est accueilli pendant 18 mois au sein de la clinique privée la plus importante du pays, la Mayo Clinic, à Rochester, dans le Minnesota.
Recruté par le CNRS, à son retour, il rentre à Rennes, où il participe à la création d’une unité INSERM, qu’il intègre pour travailler sur les problèmes de fusion d’images. Il y restera, rejoignant dans les années quatre-vingt-dix l’équipe VISTA, de l’IRISA, une unité mixte INRIA-Rennes, CNRS, Université de Rennes 1, INSA de Rennes.
Au sein de VISTA, Christian Barillot poursuit ses recherches sur l’imagerie médicale, un thème qui prend de plus en plus d’importance dans l’équipe jusqu’à ce qu’en 2004, il monte son propre projet de recherche, VISAGES.
Dès ses travaux de thèse, Christian Barillot a choisi de travailler au plus près des équipes médicales. C’était au début des années quatre-vingts, ses recherches, encadrées par le Professeur Scarabin, neurochirurgien, portaient sur la synthèse d’images et ses applications à l’imagerie médicale. Depuis, ce thème est resté son domaine de prédilection et dans le projet VISAGES qu’il a créé en 2004, il concentre ses travaux sur les pathologies de la tête et du cou.
Aujourd’hui, ses recherches le conduisent en salle d’opérations, en neurochirurgie, autour d’un enjeu : des images, acquises pendant l’intervention, et fusionnées avec d’autres images acquises auparavant, pourraient-elles apporter aux chirurgiens des informations visuelles plus précises et plus complètes que ce qu’ils observent eux-mêmes ?
La médecine et la chirurgie utilisent des images multiples, qui sont basées sur des techniques totalement différentes. L’échographie utilise le son pour tracer une topologie. L’IRM (imagerie par résonance magnétique) fournit une description géométrique, basée sur l’observation des propriétés magnétiques des tissus. Associer les deux revient à additionner des choux et des carottes. La fusion d’images est pourtant un domaine d’expertise où plusieurs équipes ont fait progresser la connaissance.
Dans chaque type d’imagerie, on recherche des informations communes – puisque la réalité observée est la même. Ces informations permettent d’élaborer des modèles. Ce sont ces modèles qui servent ensuite à intégrer des informations provenant d’une source dans l’image issue d’une autre technique, pour la compléter.

Recalage de données cérébrales : superposition de sillons corticaux.
La précision, en profondeur
La neurochirurgie est affaire de précision. On ne taille pas au hasard dans le cerveau humain, c’est pourquoi le chirurgien prépare son intervention avec des images acquises avant l’opération, par imagerie par résonance magnétique (IRM) notamment. Toutefois, la topologie du cerveau évolue, avec l’anesthésie, la pression artérielle, etc. Plusieurs études internationales ont montré que l’ouverture de la boîte crânienne, sans intervention directe sur le cerveau, pouvait entraîner des modifications de topologie de plus d’un centimètre.
Ces changements sont lourds de conséquences pour le neurochirurgien, qui travaille au millimètre près. La préparation de l’intervention doit être réajustée pendant l’opération, mais si le chirurgien peut voir les modifications de surface, il n’a pas la vision de ce qui se passe en profondeur.
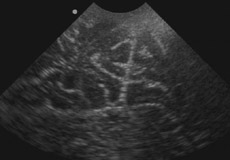
Échographie intra-opératoire de sillons corticaux.
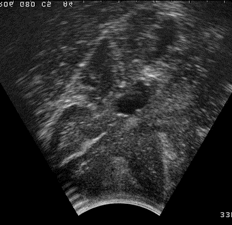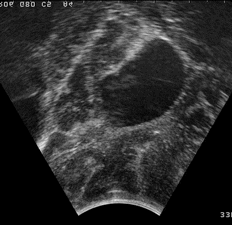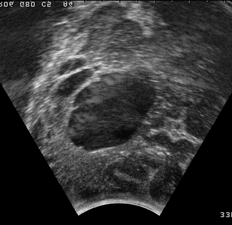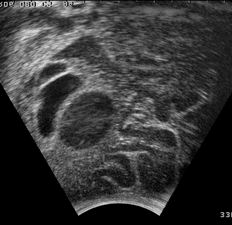
Autre exemple d’image échographique : séquence d’échographie 3D peropératoire d’une tumeur au cerveau.
L’échographie pourrait être utilisée en salle d’opération et donner cette information, jusqu’à 10 cm de profondeur, mais elle reste moins facile d’interprétation que l’IRM, qui reste à ce jour difficile à mettre en œuvre pendant l’opération. Christian Barillot veut associer les deux : utiliser des informations données par l’échographie pendant l’opération pour modifier, en temps réel, les images IRM acquises avant, y compris sur le volet fonctionnel. Cet objectif pose plusieurs problèmes scientifiques aux chercheurs.
La fusion d’images est un thème de recherche désormais classique. L’équipe de Christian Barillot se spécialise sur l’adaptation de l’image échographique, en vue de son intégration à l’image IRM. Grâce à l’utilisation de mesures statistiques et une modélisation du signal échographique recueilli, on peut améliorer l’intégration des informations obtenues dans l’image IRM.
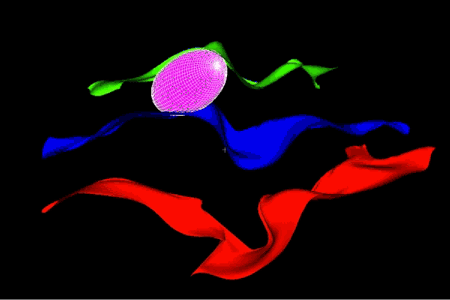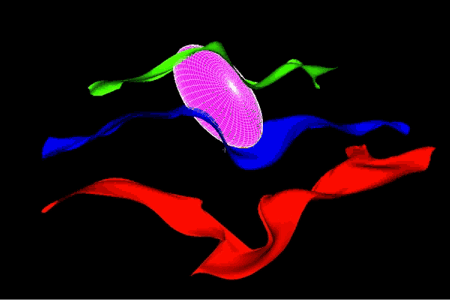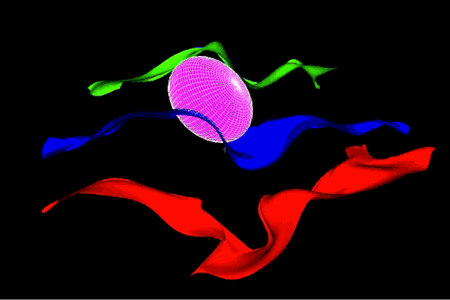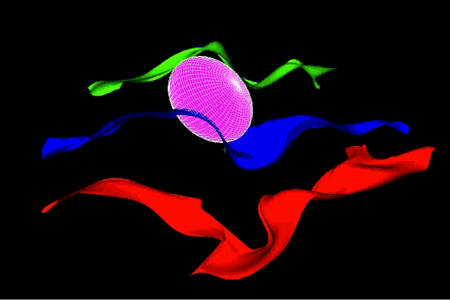
Variabilité de la somatotopie des doigts de la main droite sur une population d’individus.
La somatotopie est la cartographie des régions sensorielles primaires du cerveau.
Sur cette image, le volume rose correspond à la probabilité de localisation de l’activité fonctionnelle des doigts de la main (respectivement pouce, index, annulaire).
On constate que cette localisation change en fonction des doigts activés (la zone correspondant au pouce est celle la plus à droite dans l’image). Cette probabilité est calculée sur la base d’une population d’apprentissage.
Le deuxième enjeu est lié au temps réel. En cours d’opération, l’image IRM transformée par l’observation échographique doit être instantanément disponible pour le chirurgien. Les calculs informatiques nécessaires doivent être rapides. L’équipe travaille sur la conception d’algorithmes de traitement plus efficaces et sur leur parallélisation ou interopérabilité avec des sites cliniques partenaires. Là encore, Christian Barillot peut s’appuyer sur les travaux d’autres équipes, notamment ceux consacrés à la médiation d’informations et au « grid computing ». Les recherches sont d’autant plus importantes dans ce domaine que cet enjeu – le temps réel et l’efficacité des calculs – concerne l’ensemble de la robotique médicale.
La sécurité informatique est le troisième axe de recherche. Il faut garantir (c’est-à-dire valider, car la démonstration rigoureuse, au sens mathématique, est impossible) qu’à tout moment, l’image fusionnée est fiable et pertinente. Ce qui ne serait pas important sur une application de loisirs, devient vital dans le domaine de la chirurgie. Il ne s’agit pas de faire de son mieux, mais de prouver que le résultat est garanti.
Si la chirurgie est très ouverte aux nouvelles technologies, leur mise en œuvre implique toutefois de nombreuses expérimentations, de façon à apporter la preuve de leur fiabilité.
Garantir la fiabilité et la pertinence des méthodes développées exige un long travail préalable de validation de ces méthodes. Cela passe par des travaux sur l’étude de la stabilité et de la précision des méthodes, en utilisant des fantômes de calibration, ou bien des données avec « vérité terrain » déjà connue (modèle mathématique, définition de la « vérité » par un ou plusieurs experts…). Ensuite, cela doit être validé en clinique, sur des patients ayant à la fois une procédure normale, et la nouvelle méthode à expérimenter.
Actuellement, des tests sur l’acquisition d’images échographiques au cours de l’intervention sont conduits pendant différentes opérations sur des tumeurs bénignes au centre hospitalier de Rennes. De même, la reconstruction d’images intégrant les deux sources (échographique et IRM) est également en cours d’expérimentation. L’étape suivante portera sur la restitution en temps réel de ces images fusionnées au chirurgien.
La modélisation des gestes chirurgicaux
L’introduction de ces technologies entraîne une modification dans la pratique des chirurgiens, notamment dans l’organisation d’une intervention. Les capteurs échographiques introduisent une nouvelle contrainte dans l’environnement chirurgical. C’est pourquoi, parallèlement aux recherches sur l’imagerie, l’équipe de Christian Barillot s’intéresse à la modélisation de cette nouvelle pratique : identifier toutes les entités intervenant au cours d’une intervention, décrire les relations entre ces entités, les gestes nécessaires et définir l’assistance, les paramètres ou les outils dont aura besoin le chirurgien pour lancer telle ou telle procédure. Un tel modèle pourrait ensuite être utilisé pour la formation des chirurgiens.
Les problèmes rencontrés par les chirurgiens et leurs besoins sont les principaux moteurs des recherches de Christian Barillot qui a tissé à Rennes et dans la région des partenariats de travail avec différentes équipes médicales. C’est important pour identifier les problèmes et réorienter les travaux en permanence. En effet, il peut se passer 15 ou 20 ans entre le moment où une recherche est lancée et le moment où elle est adoptée dans la pratique clinique.
Niveau de lecture
Aidez-nous à évaluer le niveau de lecture de ce document.
Votre choix a été pris en compte. Merci d'avoir estimé le niveau de ce document !
