Projet Shamash : production de biocarburants lipidiques par des microalgues
La fin du pétrole… chacun en a entendu parler. Et la production d’agrocarburants, annoncée un temps comme la solution miracle, montre aujourd’hui ses nombreux inconvénients. Une nouvelle voie fait l’objet de recherches prometteuses, la production de carburants lipidiques par des microalgues.
En France, de telles recherches sont menées par le projet Shamash, présenté dans cette vidéo.
Quel est dans ce cadre l’apport spécifique des mathématiques appliquées ?
Comprendre et optimiser la production de biocarburant par des microalgues
Certaines microalgues ont des propriétés particulièrement intéressantes : une partie du CO2 incorporée dans leur biomasse à l’aide de l’énergie solaire est transformée en huile. Ainsi, certaines espèces peuvent contenir jusqu’à 80 % de leur masse en huile, laquelle peut servir de carburant au même titre que celle de colza ou de tournesol.
Microalgue Pseudonitzschia Calliantha vue au microscope.
Les lipides ont été colorés par un fluorochrome (le rouge du Nil). Les réserves d’huile utilisable directement sous forme de biocarburant sont colorées en jaune.
© Photo IFREMER Nantes.
Les avantages sont impressionnants puisque, de par leur forte croissance (la biomasse peut doubler chaque jour), les microalgues pourraient, dans la décennie à venir, avoir des rendements théoriques 30 fois supérieurs aux agrocarburants actuels, et ce, sur des surfaces qui n’entrent pas en concurrence avec l’agriculture alimentaire.
Mais les choses ne sont pas aussi simples : lorsqu’elles produisent d’importantes réserves lipidiques, généralement sous l’effet d’un stress, ces algues arrêtent de se diviser. Il faut donc trouver un compromis entre la croissance de la population d’algues et l’accumulation transitoire des réserves énergétiques au sein de chacune d’elles.
Le projet Shamash, financé par l’Agence Nationale de la Recherche, et coordonné par Olivier Bernard, chercheur à l’Inria Sophia Antipolis Méditerranée, a pour but la production de biocarburant sous forme d’ester de méthyl à partir de microalgues. Son objectif premier est d’évaluer la faisabilité technico-économique d’une telle filière, en créant une synergie entre les différentes expertises.
Le chemin est long pour parvenir à un mode de production à grande échelle économiquement viable. Sélectionner les variétés d’algues les mieux adaptées, étudier les paramètres de leur croissance, analyser la composition de l’huile, définir les modalités d’extraction, vérifier la qualité du carburant produit… à chacun de ces stades, modélisation et expérimentation se répondent pour choisir les meilleures solutions.
Shamash intègre pour cela des spécialistes de la culture, de la physiologie et de l’utilisation de microalgues, des spécialistes de l’optimisation des procédés biotechnologiques, ainsi que des spécialistes des biocarburants et de l’extraction et de la purification de lipides. Ce projet, d’un budget total de 2,8 millions d’euros, implique 7 équipes de recherche, issues de plusieurs organismes de recherche, Inria, CNRS, IFREMER, CEA, CIRAD, et des universités de Nantes et d’Aix en Provence, ainsi que deux industriels, Valcobio et Alphabiotech.
Dans ce cadre, l’équipe COMORE de l’Inria Sophia et le Laboratoire d’Océanographie de Villefranche cherchent à comprendre et de quantifier les mécanismes physiologiques sous-jacents, afin de définir les conditions optimales de production d’huile tout en maintenant une forte croissance des algues. La modélisation numérique est pour cela un élément capital.
Induire le stockage de lipides et gérer le compromis entre bioproduction et croissance

Photobioréacteurs expérimentaux pilotés par ordinateurs.
LOV, Villefranche-sur-mer.
Le stockage de lipides résulte d’un déséquilibre transitoire entre le flux de carbone issu de la photosynthèse et le flux d’autres éléments nécessaires à la croissance (phosphore ou azote). La cellule, qui est carencée en l’un de ces éléments, n’interrompt pas immédiatement l’acquisition du CO2 nécessaire à la photosynthèse, alors qu’elle ne peut pas l’utiliser pour construire des protéines puisque, par exemple, l’azote est manquant. Elle doit donc stocker ce flux, et chez certaines espèces, ce stockage a lieu principalement sous forme de lipides. Les recherches menées dans l’équipe COMORE en collaboration avec le Laboratoire d’Océanographie de Villefranche-sur-mer du CNRS ont pour objectif de calculer les conditions de stress à appliquer pour stimuler cette production de lipides.
Les chercheurs de l’équipe COMORE ont pour cela développé des modèles capables de prédire, en fonction des réserves de la cellule et de son environnement, le flux de carbone qui sera stocké sous forme d’huile. Ce modèle dynamique est ensuite utilisé, à l’aide de techniques issues du contrôle optimal, pour calculer, à chaque instant, le stress nutritionnel à imposer à la cellule. Les calculs doivent nécessairement tenir compte du fait qu’une carence nutritive réduit, voire arrête, la croissance des microalgues. Il faut donc trouver un compromis entre l’accumulation d’huile (due à la carence en azote) et une croissance forte (qui nécessite une quantité élevée d’azote). Ce compromis permettra d’optimiser la productivité, en calculant les conditions optimales qui maintiennent ces microorganismes dans un état qui, bien que non naturel, est favorable à la production d’huile.
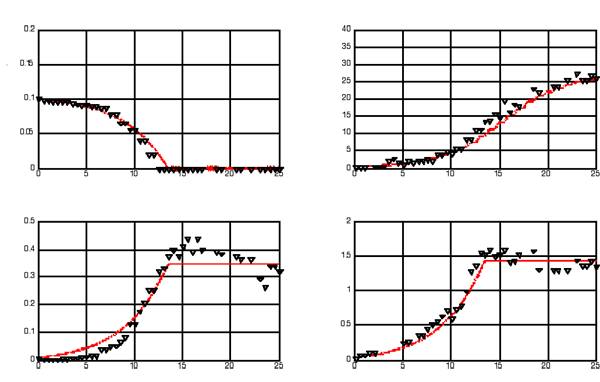
Simulation d’un modèle numérique prédisant la croissance de microalgues (substrat résiduel (ammonium), carbone et azote algaux, chlorophylle) et comparaison à une expérience avec la microalgue Isochrysis galbana.
Tenir compte des phénomènes d’atténuation de la lumière par les pigments des algues
La croissance des microalgues sous l’effet de la lumière s’effectue de façon contrôlée dans des photobioréacteurs. Lorsqu’on cultive ainsi des microalgues en photobioréacteur, on cherche généralement à obtenir des cultures très denses afin d’intensifier la concentration en huile. Or les algues contiennent des pigments, ce qui a pour conséquence d’augmenter la densité optique du milieu et le gradient de lumière entre la source lumineuse et le centre du photobioréacteur. Cela conduit à une situation non satisfaisante, où les algues à la périphérie reçoivent trop de lumière et dépensent de l’énergie pour se protéger des rayons lumineux, tandis que les algues au centre ont une croissance limitée par le manque d’énergie solaire. Les modèles numériques de microalgues, couplés à des modèles hydrodynamiques produits par le GEPEA (université de Nantes), permettent d’optimiser la géométrie des systèmes de culture pour que chaque cellule ait le meilleur accès à la lumière. La recherche de conditions optimales dans des régimes nécessairement dynamiques ne peut être menée précisément qu’en quantifiant les phénomènes à l’aide d’un modèle numérique.
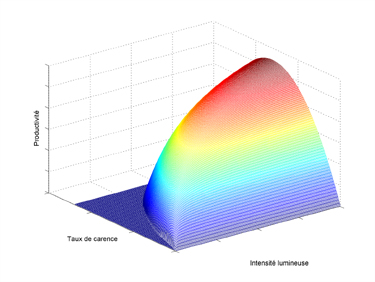
Évaluation, à l’aide d’un modèle numérique, de la productivité en huile obtenue en fonction d’un niveau de carence en azote et de l’intensité lumineuse.
Cette figure montre qu’il existe un taux de carence optimal pour une intensité lumineuse donnée.
Réguler les concentrations en CO2 et en oxygène
Pour atteindre des taux de croissance élevés en photobioréacteurs, il faut garantir que la teneur en CO2 dissous n’est jamais trop faible. En général, il ne suffit pas de faire circuler de l’air, il faut également apporter une source extérieure de CO2 (par exemple issu de gaz produit par une centrale thermique de production d’électricité). Le CO2 dissous est néanmoins un acide qui, pour des apports trop forts, peut considérablement acidifier le milieu, ce qui peut devenir létal pour les microalgues.
Il faut donc réguler l’apport en CO2 en fonction des biomasses des microalgues et de leur état (par exemple, la nuit, elles ne consomment pas de CO2). Là encore, c’est un contrôleur automatique qui opère, sur la base de la connaissance de paramètres du milieu (tels que l’alcalinité) et de l’activité biologique.
De plus, la consommation de CO2 s’accompagne, au cours de la photosynthèse, d’une production d’oxygène (la quantité d’oxygène produite est légèrement supérieure à celle du CO2 consommé). L’oxygène à forte concentration étant toxique pour la croissance, il faut en diminuer la concentration en jouant sur les régimes hydrodynamiques induits par les bulles de mélange air/CO2.
Là encore, ce sont des modèles numériques qui nous permettent, en fonction de la géométrie du photobioréacteur, de calculer les injections de gaz à réaliser pour maintenir de fortes concentrations en CO2 tout en évitant l’acidification du milieu ou sa suroxygénation.
Niveau de lecture
Aidez-nous à évaluer le niveau de lecture de ce document.
Votre choix a été pris en compte. Merci d'avoir estimé le niveau de ce document !


