La stimulation électrique au service du corps
L’électrothérapie exploite les propriétés électrophysiologiques du système nerveux. Même si les déficiences du système sensori-moteur humain sont bien connues aujourd’hui, elles restent encore trop souvent dans une impasse thérapeutique. Une voie technologique permet de restaurer ou suppléer certaines fonctions déficientes du système sensori-moteur : il s’agit de la stimulation électrique. Elle a déjà montré de grands succès comme dans le cas des stimulateurs cardiaques (pacemaker) permettant de réguler le rythme des battements du cœur, des implants cochléaires restaurant l’audition, ou même plus récemment des implants « cerveau profond » visant à supprimer les tremblements dans la maladie de Parkinson. Les progrès de la micro-électronique et de l’informatique permettent d’envisager de nouvelles applications aux neuroprothèses modernes.
L’électrothérapie désigne l’ensemble vaste et varié des utilisations thérapeutiques du courant électrique. La stimulation électrique des muscles squelettiques ou des nerfs les innervant permet d’induire une contraction des fibres musculaires et de générer une force. La stimulation coordonnée de différents muscles permet de réaliser des fonctions plus ou moins complexes : station debout, marche, préhension, etc. D’autres muscles peuvent être stimulés : le cœur et la vessie par exemple. Les voies sensitives peuvent aussi être activées par cette technique de façon à soulager une douleur ou restaurer une fonction : audition, vision… La stimulation peut être réalisée par des systèmes externes ou implantés dans le corps. Certaines applications sont une réalité clinique, d’autres restent du domaine de la recherche.
« L’Homme est une Machine si composée, qu’il est impossible de s’en faire d’abord une idée claire, et conséquemment de la définir... »
Julien Jean Offray de La Mettrie L’Homme Machine 1747
En faisant une analogie un peu grossière avec la robotique, le corps humain comporte un calculateur, le système nerveux central, une structure mécanique, le squelette, des actionneurs, les muscles, des capteurs, les récepteurs sensoriels et des câbles électriques, les nerfs. La stimulation électrique utilise les muscles comme s’il s’agissait de moteurs aux propriétés spécifiques. Bien entendu, certaines caractéristiques rendent le contrôle de ces actionneurs difficile, en particulier l’existence du phénomène de fatigue. De plus, la force maximale pouvant être produite par un muscle est notamment relative à sa longueur au moment considéré.
Un peu de physiologie
Le système nerveux humain est un système complexe dont dépendent toutes les fonctions de l’organisme. On distingue le système nerveux central (encéphale et moelle épinière) du système nerveux périphérique (nerfs). Le système nerveux central est responsable de l’émission d’influx nerveux moteurs et du traitement des informations sensitives. Le système nerveux périphérique est responsable de la transmission des influx nerveux entre les structures de l’organisme. La moelle épinière reçoit les informations sensorielles issues des récepteurs situés au niveau de la peau, des muscles et des articulations. Elle contient les motoneurones responsables des mouvements. À la moelle épinière sont reliés des nerfs essentiellement composés d’axones, qui sont les prolongements des cellules nerveuses (neurones). Les axones conduisent l’influx nerveux et assurent ainsi la propagation des messages sensoriels de la périphérie vers le centre (axones afférents) ou des incitations motrices des centres vers la périphérie (axones efférents).
Les muscles produisent le mouvement sous le contrôle du système nerveux. Les muscles sont composés de fibres qui transforment l’énergie chimique en énergie mécanique pour produire des forces. Le muscle est un tissu contractile : il est capable de se contracter en diminuant sa taille. Le corps humain comporte plus de 600 muscles. On en distingue différents types : les muscles squelettiques, le muscle cardiaque, les muscles lisses (paroi des artères, vessie, parois du tube digestif, utérus…).
Lorsqu’un motoneurone émet un influx nerveux, le groupe de fibres qu’il innerve entre en contraction ; l’ensemble constitué du motoneurone, de son axone et des fibres musculaires cibles est appelé unité motrice. Les muscles au repos sont élastiques : ils ont la propriété de s’allonger lorsqu’ils sont soumis à une force extérieure et de retrouver leur longueur initiale lorsque cette force est supprimée. Le muscle présente aussi une viscosité : sa tension passive ne dépend pas seulement de sa longueur, mais aussi de la vitesse à laquelle il est étiré. La force engendrée par le muscle est ainsi la somme des contributions mécaniques passives et de la contraction active. Cette dernière, à niveau d’activation constant, varie en fonction de la longueur et de la vitesse d’élongation ou de raccourcissement du muscle.
Toutes les fibres musculaires ne sont pas identiques, on distingue les fibres musculaires lentes et les fibres musculaires rapides, sensibles à la fatigue. La composition de chaque muscle dépend ainsi des fonctions motrices principales qu’il est censé remplir. Les fibres les plus résistantes à la fatigue sont les plus utilisées, tandis que les fibres les plus fatigables n’entrent en jeu que lorsque des forces importantes sont nécessaires.
Excitabilité électrique

Principe du galvanisme
(© Costa/Leemage)
Galvani a découvert en 1789 les propriétés de « l’électricité animale », appelée aujourd’hui électrophysiologie. Le galvanisme fait référence à l’utilisation de l’électricité sur des organismes vivants.
En 1789, Galvani observa que les muscles de la cuisse d’une grenouille se contractaient lorsque le nerf les innervant était mis en contact avec du métal. Il conclut à l’existence d’une « électricité animale ». L’étude moderne des effets galvaniques en biologie est appelée électrophysiologie. Le galvanisme se réfère à l’utilisation d’électricité sur les organismes vivants. L’œuvre de Shelley « Frankenstein » est fortement influencée par ces découvertes et pousse à l’extrême les applications du galvanisme. Des phénomènes naturels électriques étaient déjà connus et utilisés à des fins médicales durant l’Antiquité égyptienne. Certains médecins de l’empire romain utilisaient les décharges électriques générées par le poisson torpille pour traiter certaines pathologies.
Les neurones et les fibres musculaires sont des cellules excitables : elles sont capables de répondre rapidement à un stimulus par la modification brutale de charges électriques situées de part et d’autre de leur membrane.
Lorsqu’une impulsion électrique est appliquée à une fibre nerveuse par l’intermédiaire de deux électrodes, une partie de ce courant électrique pénètre dans la membrane au niveau de l’anode et ressort au niveau de la cathode. Lorsque l’intensité du courant est faible, la membrane voisinant la cathode se dépolarise partiellement. Si l’intensité du courant est augmentée progressivement, la dépolarisation augmente parallèlement jusqu’à un niveau critique de dépolarisation. Au-delà de ce seuil, la membrane devient alors le siège d’une variation de potentiel extrêmement rapide qui n’est plus contrôlée par l’impulsion électrique qui l’a déclenchée. La membrane change de polarité pendant un laps de temps de l’ordre de 1 milliseconde puis retrouve son état initial. Cette variation brève du potentiel membranaire est appelée potentiel d’action (PA) et constitue la partie essentielle de l’influx nerveux.
L’amplitude du PA est indépendante de l’intensité du stimulus, il s’agit d’un phénomène « tout ou rien ».
L’activation d’une cellule par une impulsion électrique ne dépend pas seulement de l’amplitude de l’impulsion, mais plutôt de la charge électrique vue par la cellule. Ainsi, pour chaque amplitude, une durée minimale de l’impulsion est nécessaire pour déclencher un PA dans la cellule. Pour autant, il existe une valeur seuil de l’amplitude de l’impulsion en dessous de laquelle elle ne permet jamais de déclenchement, aussi longue que soit la durée de l’impulsion. Les membranes excitables ont la propriété de propager le long de toute leur surface les potentiels d’action nés d’une stimulation localisée efficace. Un PA généré au niveau d’une zone membranaire se propage de proche en proche le long de la membrane à une vitesse constante et sans diminuer d’amplitude. Un axone innervant de nombreuses fibres musculaires (de la même unité motrice), un seul PA peut activer des centaines de fibres musculaires de façon synchrone.
Quand le système sensori-moteur est défaillant
Il existe de nombreuses situations pour lesquelles le système sensori-moteur présente des défaillances, à la suite d’un accident ou d’une maladie. Deux situations se présentent le plus souvent : les lésions médullaires (moelle épinière) et les lésions du cerveau.
Traumatisme médullaire
Le traumatisme de la moelle épinière se caractérise par des atteintes des cellules de la moelle épinière pouvant causer une paralysie et des pertes sensitives. Le traumatisme peut être dû à un accident ou une maladie. Les séquelles dépendent du niveau de la colonne vertébrale qui a été atteint : paralysie des deux membres inférieurs (paraplégie) ou des quatre membres (tétraplégie). La moelle épinière étant le lien essentiel entre le cerveau et les organes, toute atteinte de celle-ci entraîne des dysfonctionnements des organes.
En fonction du niveau de la lésion, différents organes seront touchés. Plus l’atteinte est haute, plus les conséquences physiques et physiologiques vont être importantes. Selon l’extension verticale et transversale de la lésion médullaire, la transmission des commandes volontaires de la motricité et des messages sensitifs entre encéphale et membres est plus ou moins interrompue. En cas de lésion transversale complète, les deux côtés du corps, en dessous du niveau de la lésion, sont affectés de manière symétrique. Cela signifie une absence totale d’activité musculaire volontaire et une insensibilité complète de cette partie du corps. La paraplégie correspond à une lésion de la moelle épinière au niveau thoraco-lombaire et implique une perte de la motricité et de la sensibilité des jambes et éventuellement de la partie basse du tronc. Les membres supérieurs gardent leurs fonctions et, dans les cas les plus favorables, la musculature de la respiration n’est pas touchée. La tétraplégie est due à une lésion au niveau des vertèbres cervicales, ce qui entraîne une paralysie des quatre membres et une atteinte plus ou moins grave de la musculature de la respiration.
Dans tous les cas, les muscles et récepteurs sensoriels situés en dessous de la lésion restent vivants, et les boucles réflexes spinales actives. Les muscles et récepteurs dont les voies nerveuses aboutissent au niveau de la lésion dégénèrent, tandis que les boucles réflexes spinales liées à ce niveau disparaissent. En dessous d’une lésion médullaire transversale, la motricité et la sensibilité, y compris les commandes des sphincters de la vessie et de l’anus, sont atteintes. Lors d’une paralysie incomplète, certaines fonctions résiduelles sont conservées, la rééducation fonctionnelle est alors envisageable dans certains cas, avec pour objectif le maintien et la récupération d’un maximum de fonctions.
Lésions cérébrales
Les lésions cérébrales peuvent être la conséquence d’un traumatisme crânien, d’un accident vasculaire cérébral (AVC) ou de tumeurs cérébrales. La lésion des centres moteurs peut induire des troubles de la commande volontaire des membres supérieurs et inférieurs. Une des conséquences fréquentes de l’AVC est une hémiplégie du côté opposé à l’atteinte cérébrale. Si la récupération neurologique naturelle survient dans les mois qui suivent l’AVC, avec une rééducation fonctionnelle adaptée, un handicap de marche persiste néanmoins dans 10 à 20 % des cas. Il s’agit notamment d’une incapacité à produire une dorsiflexion du pied lors de la phase de balancement (phase de vol) de la marche, le pied traîne alors au sol et gêne la progression des patients (syndrome de pied tombant ou drop-foot).
La stimulation électrique fonctionnelle (SEF)
Les cellules impliquées dans la génération de mouvement, cellules musculaires et cellules nerveuses, sont excitables. Les potentiels d’action (PA) prennent en général naissance au niveau des motoneurones situés dans la moelle épinière, derniers relais entre le système nerveux central et l’unité motrice du muscle cible. En l’absence d’entrée activatrice au niveau de ce motoneurone, plus aucune contraction n’a lieu, induisant de fait la paralysie du muscle concerné. Mais les cellules impliquées étant excitables, une impulsion électrique peut provoquer une dépolarisation de la membrane de la cellule musculaire ou de l’axone de la cellule nerveuse. Un PA peut être ainsi artificiellement produit. Il induit une contraction des fibres musculaires de l’unité motrice que l’axone innerve.
Un système de stimulation électrique comporte une source d’énergie, un circuit électronique générateur de stimuli électriques et des électrodes. Les deux électrodes sont placées sur le trajet du nerf moteur cible ou proche de la plaque motrice ou point moteur, là où les fibres nerveuses se connectent aux fibres musculaires. D’un point de vue électrique, un stimulateur génère une impulsion contrôlée en courant ou en tension, dont la largeur, la fréquence et l’amplitude sont ajustables afin de moduler la force produite.
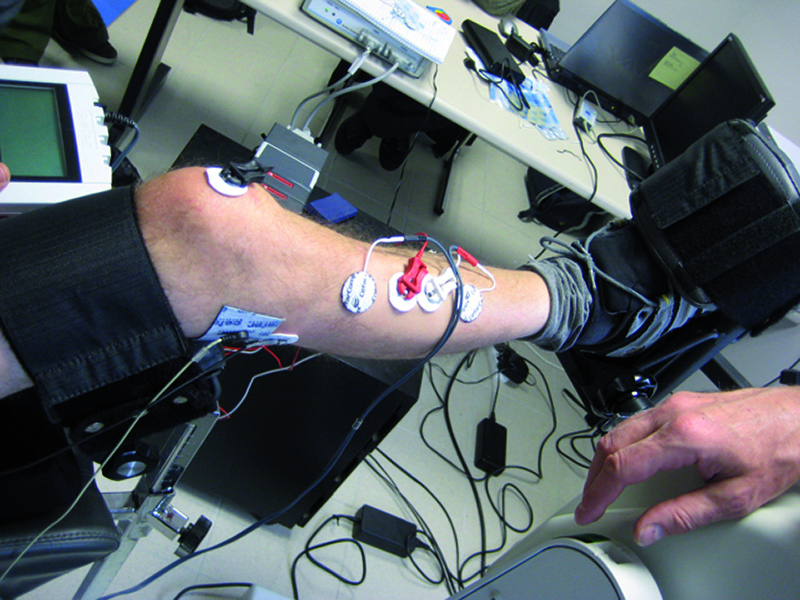
La SEF externe
Dans le cas de la SEF externe, les électrodes sont placées sur la surface de la peau recouvrant le muscle ou le nerf à activer. Les applications de cette technique sont variées : renforcement musculaire, traitement de la douleur, rééducation fonctionnelle…
La SEF est aujourd’hui pratiquée de façon courante en rééducation fonctionnelle chez les sujets lésés médullaires « incomplets » et hémiplégiques avec pour objectif une récupération de certaines fonctions. Elle permet de reproduire des mouvements de façon précise et répétable, et présente l’avantage de stimuler simultanément les voies afférentes (sensitives) et efférentes (motrices), ce qui semble favoriser la récupération. Bien que la demande de verticalisation assistée soit importante chez les patients lésés médullaires, seuls les appareillages orthétiques permettent aujourd’hui d’assurer un aplomb fonctionnel. Ces systèmes restent contraignants en termes d’encombrement et sont rarement utilisés en dehors du domicile. La stimulation électrique permet de contracter les muscles des membres inférieurs pour permettre à des sujets paraplégiques « complets » de se tenir debout. La station debout et la déambulation sont ainsi possibles, mais limitées dans le temps car il survient une fatigue musculaire précoce.

Muscles de verticalisation (© CRDP)
On peut stimuler différents muscles comme le quadriceps, le biceps fémoral ou le jambier antérieur pour permettre à des sujets paraplégiques de se mettre debout ou corriger le syndrome du pied tombant chez un sujet hémiplégique.
En France, on dénombre environ 50 000 paraplégiques et leur nombre augmente de 1 000 victimes chaque année. 80 % des victimes de traumatismes médullaires sont des hommes et 60 % ont moins de 30 ans. Près de la moitié des cas sont dus à des accidents de la route, les autres causes principales étant des accidents du travail et des accidents de sport. Aujourd’hui, la stimulation électrique reste la seule technique permettant d’activer un muscle situé sous une lésion médullaire complète. Sur le schéma sont représentés les différents muscles qui peuvent être stimulés pour verticaliser des sujets paraplégiques : (1) chef vastus latéralis du quadriceps, (2) ischio-jambier biceps fémoral, (3) grand fessier (4) jambier antérieur. Dans le cas de la correction du syndrome de pied tombant chez le sujet hémiplégique, c’est le jambier antérieur qui est principalement visé (4).
Une des utilisations courantes de la SEF est la correction du syndrome de pied tombant, très répandu chez les personnes souffrant d’hémiplégie. Il s’agit d’une incapacité à relever le pied au moment de la phase de vol
de la marche, en raison d’une faiblesse de la commande du muscle jambier antérieur. La SEF est appliquée en regard du nerf péronier qui innerve ce muscle. Le système le plus répandu utilise un capteur de type interrupteur placé sous le talon de la jambe valide pour détecter le décollement du pied, et donc l’initiation de la phase de balancement de la jambe et pour enclencher la stimulation provoquant la contraction du muscle relevant le pied. Ces deux exemples concernent les membres inférieurs, mais la technique est similaire pour les membres supérieurs. La stimulation électrique externe présente l’avantage d’être peu invasive. Elle est intéressante pour valider l’intérêt de la technique et dans le cadre de la rééducation fonctionnelle. La SEF peut, lorsque la déficience fonctionnelle persiste, constituer une assistance permanente au mouvement. Si le placement des électrodes devient alors trop contraignant et chronophage pour un usage quotidien en environnement privé, il peut être envisagé dans certains cas d’implanter le système à l’intérieur du corps du patient.
La SEF implantée
La SEF interne consiste à stimuler directement les fibres nerveuses ou musculaires en plaçant une ou plusieurs électrodes à l’intérieur du corps, au plus près des fibres à stimuler. L’un des avantages, outre le positionnement définitif des électrodes sur les sites à stimuler, est la meilleure sélectivité et l’énergie moindre nécessaire à l’activation. Certaines applications de cette technique sont bien connues et maîtrisées comme la suppléance du rythme cardiaque (pacemaker), et la simulation du nerf phrénique pour activer le diaphragme, principal muscle inspiratoire, la restauration de l’audition (implant cochléaire). En fonction des applications, l’ensemble du système peut être implanté ou seulement une partie (stimulateurs, électrodes, capteurs, etc.). La SEF implantée permet par exemple de contrôler les membres inférieurs de patients paraplégiques.
Ainsi, l’architecture de stimulation implantée conçue dans le projet européen SUAW (Stand up and walk) est composée d’un contrôleur externe, d’un stimulateur et d’un ensemble d’électrodes implantées. Le contrôleur externe transmet, par liaison inductive (radio fréquence, RF), l’énergie et les données au stimulateur implanté au niveau de l’ombilic. Ce dernier génère les stimuli à destination des électrodes auxquelles il est connecté par des liaisons filaires. Ces liens nécessitent d’une part une opération chirurgicale très lourde et limitent forcément le nombre de canaux et donc d’activateurs. Le stimulateur possède 16 canaux. Les muscles cibles principaux sont ceux permettant la flexion, l’extension et l’abduction de la hanche, la flexion et l’extension du genou, et enfin la dorsiflexion de la cheville. Cette technologie permet d’assurer à un patient paraplégique complet une station debout et une déambulation rudimentaire aidée d’un déambulateur.
Une autre application concerne le contrôle du jambier antérieur pour la correction du syndrome de pied tombant. Le système ActiGait, proposé par Neurodan A/S, repose sur une architecture comprenant une partie implantée avec une électrode posée sur le nerf péronier et connectée à un générateur de stimuli doté d’une antenne inductive, une partie externe avec une unité de contrôle transmettant énergie et données au circuit implanté, ainsi qu’un capteur de contact pied/sol porté sous le talon qui communique par liaison RF avec l’unité de contrôle.
La fatigue musculaire, un défi
La stimulation électrique fonctionnelle est une méthode efficace pour restaurer, suppléer ou rééduquer une fonction motrice. La qualité du résultat fonctionnel reste néanmoins très variable et dépend largement de l’état physiologique (et psychologique) de la personne, mais aussi des technologies mises en œuvre. La stimulation électrique fonctionnelle, qu’elle soit externe ou implantée, pose le problème de la fatigue musculaire précoce. Il s’agit ici du premier défi à relever. En effet, les stimuli artificiels activent en premier les fibres de gros diamètre, qui sont dans le processus physiologique naturel atteintes en dernier. Ce sont les fibres les plus fatigables. Des travaux de recherche sont en cours pour proposer des solutions à ce problème, d’une part en proposant de nouvelles générations d’électrodes multi-contacts et d’autre part en développant de nouveaux patrons de stimulation électrique, de façon à doter les systèmes de capacités de sélectivité spatiale et typologique, afin de stimuler certains types de fibres plutôt que d’autres. Les fibres les moins fatigables pourraient ainsi, à terme, être mises à contribution. Ces solutions permettraient également d’activer des fibres plutôt que d’autres dans un nerf (fibres sensitives plutôt que motrices, fascicules particuliers d’un nerf).
- C.F Roques Pratique de l’électrothérapie Springer
- P. Bessou Physiologie humaine, le système nerveux Tome 1. Simep Editions (1978)
Cet article est paru dans la revue DocSciences n°13 Informatique et médecine, éditée par le CRDP de l’Académie de Versailles en partenariat avec l’Inria.
Niveau de lecture
Aidez-nous à évaluer le niveau de lecture de ce document.
Votre choix a été pris en compte. Merci d'avoir estimé le niveau de ce document !

Christine Azevedo Coste
Directrice de recherche Inria au sein du Laboratoire d'Informatique, de Robotique et de Microélectronique de Montpellier (LIRMM), responsable de l'équipe de recherche CAMIN.