Le corps : vues de l’intérieur
Molière, Le malade imaginaire
Que de chemin parcouru depuis… L’imagerie médicale a révolutionné la pratique médicale, en permettant une véritable vision de l’intérieur du corps. La première image radiologique date de 1895, lorsque le physicien allemand Wilhelm Conrad Röntgen a découvert le principe des rayons X, pour lequel il a obtenu le prix Nobel en 1901. Ces rayons, appelés X car ils étaient alors inconnus, ont la propriété de traverser les tissus biologiques, en étant atténués en fonction de la densité de ces tissus et des épaisseurs traversées. Leur impact sur une plaque photographique permet alors de « voir » les différents tissus traversés. L’histoire raconte que la première image est celle de la main de madame Röntgen.
De la radio à l’IRM
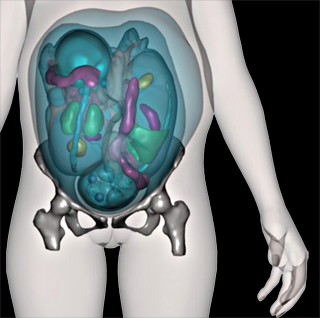
Le développement de nouvelles techniques d’imagerie médicale permet d’anticiper des opérations ou l’évolution des maladies. Ces images en 3D permettent d’avoir une vision du corps humain sans l’ouvrir et ainsi, mieux comprendre son fonctionnement.
Ces exemples résultent de travaux menés dans l’équipe Traitement et interprétation des images (Télécom ParisTech – CNRS LCTI), en collaboration avec des services hospitalo-universitaires et des industriels. Cette image a été obtenue à partir d’images IRM acquises à l’hôpital Saint-Vincent de Paul (prof. Catherine Adamsbaum, CHU Bicêtre) et d’un modèle synthétique de femme fourni par Daz Studio.
© IRM hôpital Saint-Vincent de Paul – Daz Studio.
La multiplication des modes d’imagerie médicale et les méthodes de traitement et d’interprétation fournissent une aide cruciale aux experts médicaux. Ces techniques sont utilisées pour modéliser le corps humain afin de suivre un patient (ici un exemple de fœtus jumeaux obtenus par segmentation d’images IRM 3D, pour prédire les meilleures conditions de l’accouchement ou identifier des pathologies potentielles). Elles peuvent aussi permettre de reconnaître et mesurer des structures dans le cerveau à partir d’images utilisant l’imagerie par résonance magnétique (IRM). Il peut s’agir de détecter une pathologie dans le cerveau en IRM ou dans le thorax en combinant images scanner et tomographie par émission de positons (TEP), d’estimer la position de cette pathologie par rapport aux structures normales pour guider un acte chirurgical ou une radiothérapie, ou encore de suivre son évolution au cours du temps.
Les évolutions de la technique ont permis, d’une part, de mieux contrôler les doses de rayons X et les conditions d’acquisition, afin de limiter les effets qui pourraient être nocifs pour le patient, et, d’autre part, de réaliser des acquisitions pour plusieurs directions d’incidence des rayons X. Les techniques mathématiques et informatiques dites de reconstruction permettent alors d’obtenir des images de coupes du corps humain, puis de véritables images tridimensionnelles, donnant en chaque point de l’espace la densité du tissu présent en ce point. Il s’agit de la tomodensitométrie (ou scanner X), développée en 1972 par les radiologues britanniques Allan Mc Cornack et Godfrey N. Hounsfield.
Par la suite, différentes modalités d’imagerie médicale ont été inventées, reposant sur des principes physiques différents, et mettant en avant différents aspects de l’anatomie ou des fonctions du corps. Ainsi, la découverte des phénomènes de propagation des ondes ultrasonores au début du XXe siècle a permis au cardiologue suédois Inge Edler d’obtenir la première image échographique. Ici, ce sont surtout les interfaces entre différents tissus et la manière dont elles réfléchissent les ondes ultrasonores qui sont à l’origine des images. L’imagerie par résonance magnétique (IRM), plus récente, repose sur la découverte par Edward Purcell et Felix Bloch de la résonance des noyaux atomiques (protons de l’eau qui représente 70 % des éléments du corps humain) lorsqu’ils sont soumis à un champ magnétique. Le véritable démarrage de cette modalité d’imagerie, qui met en évidence les propriétés de relaxation des tissus après une excitation par un champ magnétique, date des années 1980. Citons enfin l’imagerie nucléaire, qui s’est développée depuis les années 1990 avec la scintigraphie puis la tomographie par émission de positons. Les images mesurent la consommation par les tissus d’un produit radioactif injecté au patient, et donnent donc des informations métaboliques et fonctionnelles, et non directement des informations anatomiques.
Nos tissus sous toutes les coutures
Toutes ces techniques connaissent depuis leur invention un essor important, pour des indications de plus en plus variées. Pour ne citer que quelques exemples en IRM, des évolutions de la technique et des protocoles d’acquisition ont donné accès à des informations sur les vaisseaux sanguins, par la technique d’angiographie par résonance magnétique, à des informations sur les zones actives dans le cerveau lorsque le sujet effectue certaines tâches (sensorielles, motrices, cognitives…), par la technique d’IRM fonctionnelle, ou encore à des informations sur les faisceaux de fibres tissulaires, par exemple dans la matière blanche, par l’IRM de diffusion. Les supports de l’information ont évolué vers des supports numériques. La taille des données d’imagerie est souvent très importante (plusieurs dizaines à plusieurs centaines de mégaoctets pour un examen).
La complexité du corps humain et de sa vision par des techniques d’imagerie médicale nécessite le développement de méthodes et d’outils de traitement et d’interprétation d’images répondant à cette complexité.
De la reconstruction à l’interprétation
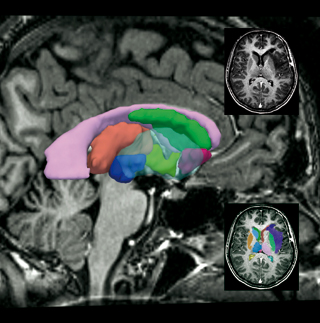
Exemple de reconnaissance de structures cérébrales pathologiques à partir d’un modèle de l’anatomie.
Le mélange de plusieurs techniques d’imagerie médicale (IRM et 3D) aide à préciser et mieux appréhender certaines maladies. Ces images et le savoir des experts médicaux pour les interpréter permettent de mieux soigner les patients.
© Olivier Nempont, images IRM hôpital Sainte-Anne.
Cet exemple montre une approche globale utilisant un réseau de contraintes spatiales. Les structures segmentées et reconnues sont montrées avec des couleurs différentes et superposées à des coupes d’images IRM. La première image (en haut à droite) est une coupe du volume IRM original. Sur la deuxième image (en bas à droite), le résultat de segmentation a été superposé à l’image originale, montrant la reconnaissance des structures internes et de la tumeur. Enfin, la troisième image est la représentation 3D des résultats de reconnaissance pour les noyaux caudés, les putamens, les ventricules latéraux, les thalami, le troisième ventricule, les noyaux accumbens et les sous-thalami. Il s’agit d’un cas pathologique, dans lequel une tumeur (le résultat de la segmentation est en violet) a fortement déformé certaines structures, qui sont toutefois bien segmentées grâce à l’utilisation de relations spatiales.
Les applications en imagerie médicale ont bénéficié des avancées du domaine du traitement et de l’interprétation des images de ces dernières années. Les outils et méthodes permettent ainsi de répondre à des objectifs très variés, de la reconstruction à l’interprétation. La plupart des images médicales, en particulier tomographiques, étant des images calculées, l’obtention d’images interprétables par le médecin ou l’ordinateur nécessite de mettre en œuvre des techniques dites de reconstruction, pour passer du signal brut issu des systèmes d’acquisition à des images numériques.
Une fois les images reconstruites, des techniques d’amélioration des images peuvent être appliquées, afin d’augmenter le contraste ou de diminuer le bruit. La difficulté de cette étape est d’adapter le traitement aux propriétés du signal et à l’utilisation qui va en être faite. Par exemple, filtrer une image pour améliorer la visualisation ou filtrer une image pour faciliter une segmentation automatique ne font pas appel aux mêmes critères de qualité du résultat, et donc sont souvent réalisés par des méthodes différentes.
Préciser les contours
Une étape-clé est ensuite la segmentation, permettant d’extraire dans les images des contours ou des régions homogènes, afin de délimiter des organes particuliers ou des régions pathologiques (tumeurs par exemple). La reconnaissance de ces structures (ou leur étiquetage en accord avec une terminologie médicale) est également un objectif primordial. Bien que ces thèmes de recherche soient déjà anciens, ils suscitent toujours beaucoup de travaux, tant les problèmes rencontrés sont difficiles et évoluent avec les techniques d’acquisition. Ils concernent à la fois les structures normales et pathologiques, ainsi que des zones relatives à des fonctions en imagerie fonctionnelle. Les méthodes fondées sur des modèles sont de plus en plus développées. En effet, la complexité des données 3D en imagerie médicale nécessite le développement de modèles intégrant de multiples connaissances et de grandes quantités d’informations, ainsi que des contraintes topologiques, géométriques ou morphologiques. Par exemple, une méthode de segmentation de vaisseaux sanguins utilisera l’information de forme tubulaire de ces structures.
La reconnaissance de structures dans les images médicales peut s’appuyer sur la modélisation des relations spatiales et leur intégration dans des méthodes de segmentation et de reconnaissance. En effet, ces relations sont largement utilisées dans les descriptions anatomiques, souvent sous forme textuelle, et ont la propriété d’être relativement stables d’un sujet à l’autre, même dans les cas pathologiques. Ce n’est pas le cas des propriétés de forme des structures, qui sont sujettes à beaucoup plus de variabilité. Prendre en compte ces relations (topologiques, métriques, d’orientations relatives, etc.) permet de s’appuyer fortement sur les connaissances anatomiques, et de reconnaître des structures qui se distinguent mal les unes des autres par leurs seules propriétés de niveaux de gris ou de forme. Cela nécessite de développer des modèles mathématiques de ces relations, en accord avec leur sémantique, puis de les rendre opérationnels dans des algorithmes de traitement et d’interprétation d’images. Une approche consiste à rechercher d’abord les structures les plus faciles à segmenter et à reconnaître dans les images, puis à rechercher les autres de manière séquentielle, en limitant la recherche aux zones de l’espace qui satisfont les relations spatiales données dans les modèles anatomiques par rapport aux structures déjà reconnues. Une autre approche consiste à exprimer toutes les relations entre structures dans un réseau de contraintes, puis à rechercher un ensemble de structures dans les images qui satisfont ces contraintes. Ces approches, qui permettent d’associer des modèles génériques à des données individuelles d’imagerie, ont été appliquées à différentes parties du corps, en imagerie thoracique ou en imagerie anténatale par exemple, avec des modèles anatomiques spécifiques de ces régions.
Mettre en commun les données
Les modèles peuvent aussi être de nature statistique. La constitution de bases de données importantes d’images dans de nombreuses équipes autorise l’emploi d’outils statistiques pour élaborer des modèles d’apparence qui prennent en compte la variabilité anatomique ou fonctionnelle dans une population. Récemment, des modèles de l’agencement spatial des structures ont été développés. Dans ces problèmes de segmentation et de reconnaissance de structures, la question de la validation reste centrale et sans solution définitive. Des séries d’images annotées et segmentées par des experts peuvent servir de base à cette validation, mais demandent à être étendues.
De plus, la notion de qualité de la segmentation a un sens qui dépend des objectifs et de l’utilisation des résultats. Cela justifie alors la définition de protocoles de validation ou d’évaluation rétrospective, en fonction des étapes ultérieures. Enfin, des mesures absolues ne sont pas toujours nécessaires : par exemple, le suivi de l’évolution d’une pathologie s’appuiera plus sur des mesures relatives, permettant de mettre en évidence des tendances dans l’évolution. Les contraintes sont alors moins fortes pour les algorithmes et plus réalistes.
La segmentation et la reconnaissance, effectuées le plus automatiquement possible, évitent des contourages manuels fastidieux et parfois peu reproductibles, et permettent d’accéder à des mesures quantitatives (volume d’une pathologie ou de sa variation au cours du temps par exemple), en s’affranchissant de la variabilité intra et inter-utilisateurs. Elles bénéficient de l’utilisation de modèles, et inversement elles permettent la constitution de modèles 3D du corps humain (voire 4D pour les organes en mouvement tels que le cœur), soit du point de vue anatomique, soit du point de vue fonctionnel. Ces modèles ont de multiples applications, allant de l’aide à la compréhension de la structure et du fonctionnement de certains organes (cœur, cerveau par exemple), à la simulation d’actes médicaux (accouchement, interventions chirurgicales, planification de radiothérapie…). Leur constitution s’appuie souvent sur l’utilisation de données multimodales et de leur fusion.
Ce domaine est fortement pluridisciplinaire, ce qui en fait l’intérêt et stimule la recherche. Il nécessite des interactions fortes entre physique, mathématiques, informatique, biologie et médecine. Les aspects déontologiques et éthiques sont également présents, ainsi que la sécurité pour le patient. Les enjeux sont majeurs puisqu’il s’agit de fournir une aide au diagnostic, au suivi des patients, à la prise de décision thérapeutique ou chirurgicale.
Le mot « aide » est ici important. Il ne s’agit pas de remplacer les experts médicaux mais de leur apporter un soutien méthodologique et informatique, leur permettant de mieux exploiter les informations contenues dans les images. Ces images proviennent de patients, il est donc important que les experts médicaux valident les résultats fournis par les ordinateurs. Même si les outils intègrent la variabilité ainsi que les difficultés pouvant provenir des mouvements du patient ou de certains organes et des déformations des tissus mous, il ne faut pas oublier le caractère individuel et unique des données obtenues pour chaque patient, l’humain avant tout.
- « Informatique et médecine », revue Docsciences n°13, CRDP de l’académie de Versailles, octobre 2010.
- Page personnelle d’Isabelle Bloch contenant des cours, des images, etc.
Cet article est paru dans la revue DocSciences n°15 Entre les hommes et les machines : automatique et traitement du signal, éditée par le CRDP de l’Académie de Versailles, en partenariat avec Inria et le CNRS, à l’initiative du comité éditorial d’Interstices.
Niveau de lecture
Aidez-nous à évaluer le niveau de lecture de ce document.
Votre choix a été pris en compte. Merci d'avoir estimé le niveau de ce document !
