La simulation en radiologie interventionnelle
Si certains enfants rêvent d’être vétérinaires-footballeurs, le neuroradiologue interventionnel a sans doute désiré être médecin-plombier. Mais attention, pas n’importe quel médecin car, comme le préfixe « neuro » l’indique, celui-ci s’attaque principalement aux pathologies vasculaires cérébrales. Pas n’importe quel plombier non plus : imaginez que vous ayez un problème dans vos canalisations de salle de bain, à l’étage ; ce plombier va s’installer à la cave, et effectue sa réparation de là. C’est en effet depuis l’aine, située à environ un mètre du cerveau, que le super médecin-plombier manipule des micro-outils qu’il conduit à travers le réseau vasculaire jusqu’à la pathologie pour la traiter. Cette procédure requiert, de la part de celui qui l’effectue, une connaissance approfondie et une maîtrise totale de ses outils, une grande attention aux subtiles réactions du patient, et enfin une longue expérience pour aborder une importante variété de cas thérapeutiques. Ce geste médical est éminemment technique, difficile et risqué, comme l’est le pilotage d’un avion de ligne. Suivant cet exemple fondateur, la simulation numérique se tourne aujourd’hui, pleine de promesses, vers le domaine chirurgical.
La simulation numérique d’un coil dans un anévrisme intracrânien (© Jérémie Dequidt / Inria)
La simulation numérique permet d’aider le monde médical à se développer, se former. Les chercheurs en géométrie, biomécanique et physiologie doivent travailler ensemble pour résoudre les problèmes frontaliers à leurs domaines.
La simulation numérique est en position de proposer des solutions pour réduire le temps de formation des personnels et en standardiser l’évaluation, accélérer le cycle de production des nouveaux matériels, notamment leur validation et réduire le temps d’examen, en proposant au médecin un environnement virtuel pour s’entraîner avant un cas difficile et tester sereinement diverses alternatives thérapeutiques. Le travail sur l’anévrisme intracrânien, que nous décrivons dans cet article, permet de cerner les éléments technologiques qu’il est nécessaire de développer pour simuler les procédures minimalement invasives traitant d’autres pathologies (sténoses, occlusion de tumeurs…) avec d’autres micro-outils (stents, ballonnets…). Simuler le vivant sur un ordinateur requiert de le modéliser géométriquement, biomécaniquement et physiologiquement. Ces trois domaines de recherche, ou plutôt les chercheurs qui y travaillent doivent donc se rencontrer et résoudre les problèmes se posant à leurs frontières communes, tant théoriquement, en développant des modèles adaptés au temps interactif, que pratiquement, en élaborant des procédés d’ajustement de ces modèles au cas particulier de chaque patient.
La simulation médicale
L’apprentissage par compagnonnage est une étape fondamentale de la formation des internes en médecine. Durant plusieurs années, elle leur permet de compléter un ensemble de connaissances « théoriques » (en anatomie, physiologie, etc.) par une maîtrise pratique d’une ou plusieurs techniques interventionnelles. C’est dans ce contexte que la simulation interactive joue un rôle croissant, en élargissant l’horizon des méthodes d’apprentissage actuelles : fréquences et horaires d’entraînements flexibles, accès à une information détaillée permettant d’analyser les causes d’une erreur, ou encore exposition à des cas pathologiques complexes dont l’occurrence est très rare lors d’une formation classique. Mais l’avantage qui reste déterminant est que ces simulations ne présentent aucun risque pour le patient, puisque celui-ci est virtuel.
Si une grande similarité existe entre simulation médicale et simulation de vol dans les objectifs et bénéfices apportés, une différence fondamentale réside cependant dans la modélisation nécessaire pour réaliser les simulations. La modélisation de la géométrie, de la biomécanique, ou de la physiologie d’une partie du corps humain est bien plus complexe que la modélisation du comportement d’un avion, et les données permettant de paramétrer ces modèles sont beaucoup plus difficiles à obtenir. Ajoutez à cela le fait que l’ensemble des calculs d’une simulation interactive doit être réalisé en quelques millièmes de seconde, et vous comprendrez que ce problème n’est pas trivial.
L’anévrisme et son traitement
Parmi les pathologies vasculaires intracérébrales, l’anévrisme est sans doute celle qui mobilise le plus d’efforts de recherche à la fois clinique et informatique. Se présentant comme une dilatation localisée de la paroi vasculaire, un peu comme une hernie sur un pneu, un anévrisme est un point faible où le vaisseau peut se rompre, provoquant une hémorragie cérébrale. Après une rupture, l’anévrisme doit être rapidement occlus. Cette occlusion, ou « embolisation », se fait le plus souvent par voie endovasculaire. Pour atteindre l’anévrisme intracrânien, le neuroradiologue interventionnel introduit un cathéter dans l’artère fémorale, au niveau de l’aine, et le conduit, en le poussant et le tournant, jusqu’aux artères du cou. Ce cathéter sert de support à un micro-cathéter, plus fin, qui peut évoluer dans l’arbre vasculaire délicat en contact direct avec le cerveau, afin d’atteindre, de manière très précise, la pathologie. Ce micro-cathéter servira à son tour de guide aux micro-outils, en particulier les coils, qui viendront occlure l’anévrisme.
Le réseau vasculaire est complexe, c’est pourquoi le médecin ne peut s’y orienter sans le contrôle visuel offert par l’imagerie par rayons X. La radiographie, doyenne des techniques d’imagerie médicale (découverte en 1895), bien qu’ionisante, et donc nocive à fortes doses, reste l’imagerie la mieux adaptée à la neuroradiologie interventionnelle. La radiographie a donné naissance, au milieu des années 1980, à l’angiographie numérique soustraite, qui permet aujourd’hui de visualiser les artères d’un patient à des cadences de 30 images par seconde, sous réserve de l’injection d’un produit de contraste. Un des principaux attraits de la radiographie est qu’elle montre le patient en transparence, sans occultation d’aucune structure anatomique. L’interprétation des images est en revanche parfois difficile, car cette transparence se fait au prix de la perte totale de l’information de profondeur. Ainsi se justifient les recherches actuelles visant à intégrer dans la salle d’opération, pour les associer étroitement au geste opératoire, des modalités d’imagerie tridimensionnelles comme le scanner, l’imagerie par résonance magnétique (IRM) ou encore l’angiographie tridimensionnelle.
La simulation de déploiement de coils
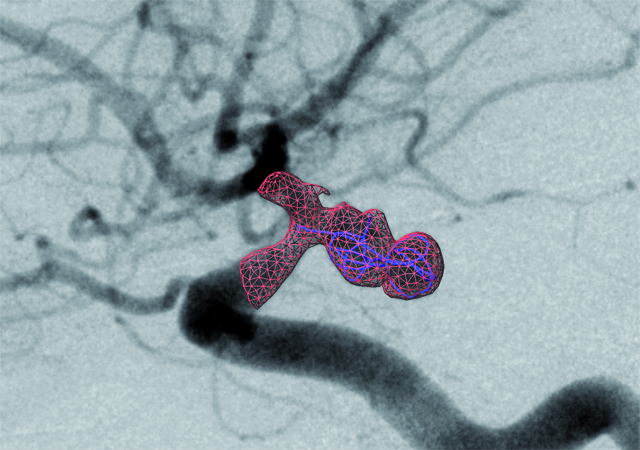
Les dessous d’une simulation (© Erwan Kerrien / Inria)
Afin de simuler le déploiement d’un coil dans un anévrisme, on utilise son modèle géométrique, animé par un modèle mécanique, placé dans un modèle des vaisseaux sanguins et en le fusionnant avec l’image réelle observée par le chirurgien.
Afin de simuler le déploiement d’un coil (en bleu sur l’illustration) dans un anévrisme, on utilise un modèle géométrique de ce coil, par exemple une liste de points reliés par des segments, que l’on anime grâce à un modèle mécanique. On place ensuite ce coil virtuel à l’intérieur d’un modèle géométrique représentant les vaisseaux sanguins (en rouge). En se déployant, le coil va venir s’appuyer sur cette surface (on parle alors de collisions) et se déformer ainsi de manière réaliste. Mais passer de cette simulation par ordinateur à la visualisation sur un simulateur demande d’accroître encore le réalisme, en fusionnant le coil simulé avec l’image réelle vue par le chirurgien. Cette image réelle, c’est l’angiographie, qui constitue ici l’image de fond, où les artères apparaissent en noir sur un fond gris clair. La surface artérielle simulée est alignée géométriquement avec les artères vues en angiographie (on parle de recalage et de fusion d’images), impliquant également l’alignement du coil. La dernière étape après l’image ci-dessus consistera à ne plus afficher la surface simulée (en rouge), donnant ainsi au neuroradiologue une image similaire à celle qu’il verrait si un coil était vraiment déployé dans l’anévrisme.
Du point de vue des chercheurs, la simulation numérique couvre de nombreuses thématiques. Parmi les plus importantes figurent la modélisation géométrique du réseau vasculaire, la modélisation mécanique des micro-outils ainsi que les interactions entre ces instruments et les vaisseaux, la modélisation des écoulements de fluides dans le système artériel ainsi que dans les anévrismes. D’autres éléments sont également nécessaires, comme la simulation réaliste des images rayons X, ou la mise en place de nouvelles techniques de parallélisme permettant d’atteindre des temps de calcul très courts même dans le cas de simulations complexes.
Le premier élément à mettre en place pour la simulation est le décor, c’est-à-dire la surface des artères au voisinage de l’anévrisme. Cette géométrie dépend totalement du patient et doit donc être extraite automatiquement, pour chaque cas, à partir des images, en particulier d’angiographie tridimensionnelle. On parle alors souvent de simulation ou modélisation « patient spécifique ». À structure complexe, modèle complexe, d’autant plus que la justesse du comportement mécanique dépend de la précision géométrique. À l’opposé, la contrainte de temps réel milite en faveur d’un modèle allégé. Le besoin de solutions innovantes, moteur de nos recherches, naît de la nécessaire conciliation de ces contraires. Le traitement virtuel d’un anévrisme requiert une autre étape clé : simuler l’interaction des différents instruments avec l’anatomie virtuelle.
Pour cela, il faut au préalable modéliser le comportement mécanique des cathéters, guides, micro-cathéters et tout particulièrement des coils. Pour que ces simulations soient réalistes, il est nécessaire d’en analyser le comportement via différents tests, puis de développer des modèles qui, non seulement restituent les aspects principaux de ce comportement, mais permettent aussi des temps de calcul très faibles. Enfin, puisque ces instruments sont en contact quasi-permanent avec la paroi interne des vaisseaux, cet élément doit être pris en compte dans la simulation. Dans le cas du déploiement d’un coil, en particulier, les contacts frottants entre le coil et la paroi de l’anévrisme vont permettre de déterminer son comportement, ainsi que la pression exercée sur la paroi de l’anévrisme.
La gestion des contacts est le lieu où géométrie et mécanique se rencontrent. Le coil est modélisé mécaniquement comme une succession de poutres flexibles. Lors d’un pas de simulation, une force, appliquée à une extrémité du coil, se propage d’une poutre à l’autre suivant les seules lois de la mécanique. Par la géométrie, la liste des extrémités de poutres en-dehors des vaisseaux est établie. Une force de rappel est alors appliquée en chacun de ces points, et la résolution mécanique est refaite. La modélisation des vaisseaux par surface implicite fournit une fonction f telle que tout point (x,y,z) extérieur à la surface satisfait f(x,y,z)>0. De plus, le gradient de f (sa dérivée) donne la direction des forces de rappel. Connaissant f, ces deux calculs sont directs et potentiellement très rapides.
Enfin, puisque le réseau vasculaire sert avant tout à la circulation sanguine, il est nécessaire de prendre en compte, dans la simulation, l’impact du flux sanguin sur la navigation des instruments, ainsi qu’à l’inverse les modifications de flux entraînées par la mise en place de systèmes endovasculaires. Cette modélisation passe par la résolution d’équations complexes, mais toujours sous la contrainte de temps de calcul très réduits.
Cet article est paru dans la revue DocSciences n°13 Informatique et médecine, éditée par le CRDP de l’Académie de Versailles en partenariat avec l’Inria.
Niveau de lecture
Aidez-nous à évaluer le niveau de lecture de ce document.
Votre choix a été pris en compte. Merci d'avoir estimé le niveau de ce document !

