Simulation de chirurgie hépatique
Considérons par exemple le développement et le perfectionnement de la chirurgie laparoscopique. Ce type de chirurgie désigne les opérations abdominales réalisées à l’aide d’instruments introduits dans l’abdomen par de petites incisions et manipulés à distance par le chirurgien. Les résections hépatiques (c’est-à-dire l’ablation de parties du foie) sont un exemple d’interventions qui peuvent être pratiquées de cette façon dans certaines circonstances.
Du gaz, généralement du gaz carbonique, est insufflé dans l’abdomen du patient pour créer un espace ouvert à l’intérieur du corps. Une caméra vidéo est insérée dans l’abdomen par l’une des petites incisions. L’image vidéo est agrandie et transmise à un écran à haute résolution qui permet au chirurgien de visualiser avec une grande acuité l’anatomie abdominale. L’intervention est réalisée à l’aide d’instruments spéciaux introduits par les autres incisions.
La chirurgie minimalement invasive présente de nombreux avantages pour le patient : une réduction de la douleur, moins de complications ultérieures, de petites cicatrices avec un faible impact esthétique, une guérison plus rapide et plus généralement une meilleure récupération du patient. Toutefois, avant de s’essayer à une telle intervention dans des conditions réelles, le chirurgien doit acquérir des compétences spécifiques et développer une coordination avancée de la main et de l’œil.
1. La simulation chirurgicale numérique
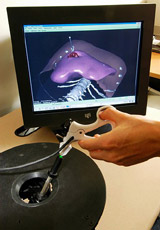
Simulation de chirurgie hépatique avec retour d’effort.
© INRIA / Photo Jim Wallace
Avant le développement de la simulation chirurgicale numérique, les médecins pouvaient s’entraîner sur des systèmes mécaniques prévus à cet effet, nommés « endotrainers », ou sur l’animal. Les endotrainers permettent au chirurgien d’utiliser les mêmes types d’instruments que ceux qui sont utilisés en chirurgie minimalement invasive, insérés par les ouvertures d’une boîte transparente. Le chirurgien peut ensuite interagir avec des objets en plastique représentant les divers organes. Ceci constitue une approximation très grossière et statique de la réalité, qui ne restitue pas la nature dynamique des tissus, la présence des vaisseaux, la vision indirecte du champ opératoire, le saignement potentiel des organes et autres facteurs. L’entraînement chirurgical sur l’animal est beaucoup plus réaliste, mais soulève un certain nombre de problèmes éthiques qui limitent sévèrement sa diffusion actuelle et future. En outre, l’utilisation d’animaux à des fins d’entraînement chirurgical reste une approche d’enseignement et de formation assez onéreuse.
En comparaison, la simulation numérique peut offrir des avantages incommensurables : la capacité à apprendre à partir de ses erreurs, la possibilité de s’exercer seul ou avec un formateur, ainsi qu’une adaptabilité supérieure permettant la simulation de divers scénarios allant des pathologies standard à des cas extrêmement rares. Mais l’intérêt des simulateurs chirurgicaux va plus loin que le simple outil de formation des internes aux modes opératoires connus des interventions minimalement invasives. En effet, les simulateurs chirurgicaux pourraient être utilisés pour répéter une intervention complexe avec les données spécifiques du patient et devenir ainsi un prolongement naturel de la planification préopératoire. Les simulateurs pourraient également servir à attester de manière quantitative et objective les compétences d’un chirurgien.
Différentes générations de simulateurs
Les simulateurs chirurgicaux peuvent être classés en trois catégories.
Les simulateurs de première génération représentent uniquement l’anatomie, en particulier la géométrie des structures impliquées dans une intervention chirurgicale. Dans ces simulateurs, l’utilisateur peut essentiellement naviguer dans une représentation virtuelle du patient, avec un jeu limité d’interactions possibles. Plusieurs simulateurs de ce type ont été développés, en particulier pour l’endoscopie virtuelle (pour des interventions de colonoscopie ou de bronchoscopie). Certains sont disponibles dans le commerce, déjà reliés à la console de traitement de certains systèmes d’imagerie tels que l’imagerie par résonance magnétique (IRM) et la tomodensitométrie (TDM). Ces simulateurs sont principalement utilisés comme outils de diagnostic complémentaires et également pour aider à la planification des interventions chirurgicales, mais ne sont généralement pas bien adaptés à la simulation des gestes chirurgicaux.
Les simulateurs de deuxième génération comprennent non seulement la modélisation géométrique de l’anatomie de l’organisme mais également la modélisation des propriétés physiques des tissus vivants. L’introduction des propriétés biomécaniques est essentielle pour permettre des interactions réalistes entre les instruments chirurgicaux et les tissus mous, y compris les déformations et les découpes. Aucun simulateur de deuxième génération n’est actuellement disponible dans le commerce, bien que de nombreux prototypes aient été développés et utilisés par plusieurs groupes de recherche, notamment pour la simulation de la résection de la vésicule biliaire et la simulation d’interventions chirurgicales en obstétrique.
Les simulateurs de troisième génération associent les modélisations anatomique, physique et physiologique c’est-à-dire la modélisation des fonctions de certains systèmes organiques tels que les systèmes cardiovasculaire, respiratoire ou digestif. À cela s’ajoute un degré de complexité lié à la nature des propriétés physiologiques et physiques. Certains modèles intéressants existent pour le système cardiopulmonaire, le système vasculaire et le système cardiaque.
Problèmes liés à la simulation chirurgicale
Un simulateur chirurgical de deuxième génération fait appel à la modélisation géométrique et physique des tissus humains pour modéliser les informations biomédicales, et restitue ces informations à l’utilisateur au travers d’une interface multimodale, avec retour visuel et haptique. Ces divers éléments font donc l’objet de recherches.
Les modèles géométriques des structures anatomiques sont, dans la plupart des cas, extraites d’images médicales en 3D (scanners ou imagerie par résonance magnétique (IRM)) avec certains outils de traitement d’image réservés à cet effet. Nous pouvons établir une distinction entre la constitution de modèles anatomiques « standard » et de modèles spécifiques à un patient. Les premiers sont utilisables dans le contexte de l’enseignement des gestes chirurgicaux pour les internes, alors que les autres sont nécessaires lorsque la simulation est utilisée pour répéter une intervention chirurgicale particulière.
La modélisation physique d’un simulateur comprend la modélisation des contacts entre les instruments virtuels et les tissus mous ainsi que la déformation biomécanique des tissus mous. Lorsqu’un choc est détecté entre une structure anatomique et un instrument chirurgical, des efforts sont appliqués sur la frontière des modèles de tissus mous et, en fonction de la nature de l’instrument, un morceau de tissu peut être prélevé. Le tissu mou est ensuite déformé selon un comportement biomécanique donné. Plusieurs modèles mathématiques ayant été proposés dans la littérature, le choix de l’un d’entre eux doit prendre en compte deux éléments antagonistes : le réalisme de la simulation et le temps de calcul pour mettre en œuvre ce modèle.
Enfin, l’interface utilisateur du simulateur chirurgical est de la plus haute importance, car il est essentiel, pour un entraînement efficace, que les chirurgiens agissent comme s’ils opéraient sur un patient réel. Les deux sens principaux qui doivent être reproduits sont la vue et le toucher. Pour produire une restitution visuelle convaincante, il est nécessaire de modéliser correctement les textures des tissus, les effets d’éclairage spécifiques d’un endoscope et différents effets spéciaux tels que les saignements. Une restitution haptique, c’est-à-dire qui donne un retour d’effort, est également un élément important pour la perception tridimensionnelle d’une intervention chirurgicale.
2. Un simulateur de chirurgie hépatique
Nous allons décrire ici certaines des phases principales du développement d’un simulateur de chirurgie hépatique, en prenant pour exemple le simulateur développé au cours des sept dernières années par l’équipe de recherche EPIDAURE de l’INRIA, en collaboration avec l’IRCAD (Institut de Recherche Contre le Cancer de l’Appareil Digestif) de Strasbourg. Notre motivation première était liée à l’importance des pathologies hépatiques et à la complexité inhérente de la chirurgie hépatique. Nous avons également pris conscience du fait que la modélisation de l’interaction avec des organes déformables de l’abdomen (en particulier du foie lui-même) constituait une gageure en matière de recherche et nous souhaitions étudier ce problème attentivement.
|
|
| Visionner une séquence vidéo qui présente notre simulateur – Durée : 2 min 15 s. |
Deux outils complémentaires ont été développés dans le cadre de ce projet. Le premier concerne la planification des interventions en chirurgie hépatique ; le deuxième est lié à la simulation des gestes et mouvements chirurgicaux. La planification des interventions hépatiques comprend principalement la détermination des segments de Couinaud (ou segments fonctionnels) qui correspondent aux zones vasculaires principales du foie. Une fois que la planification de l’intervention est réalisée, la simulation chirurgicale s’efforce de reproduire les gestes chirurgicaux avec suffisamment de réalisme pour permettre un entraînement efficace.
Modélisation géométrique
Nous avons conçu une combinaison de techniques de traitement de l’image afin d’extraire les structures hépatiques pertinentes principales à partir de scanners réalisés avant l’intervention (images préopératoires) : l’ensemble des cellules spécifiquement actives du foie (parenchyme hépatique), les vaisseaux principaux, les segments de Couinaud et les lésions potentielles. Cette extraction est réalisée en deux étapes utilisant différents modèles géométriques et différentes méthodes de segmentation d’images : en premier lieu, le parenchyme hépatique est délinéé, puis les vaisseaux ; enfin, les lésions sont détectées.
 |
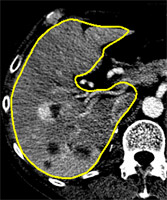 |
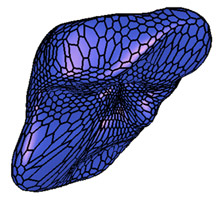
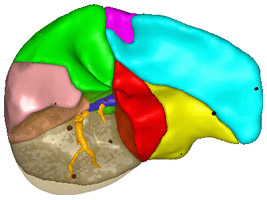
| Extraction du parenchyme hépatique à partir d’un scanner par tomodensitométrie. | |
 |
 |
|
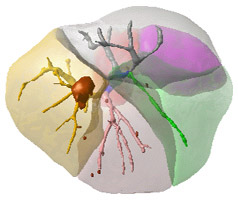
Extraction des arbres vasculaires et des lésions hépatiques à partir d’un scanner par tomodensitométrie. |
|
Ceci a abouti au premier système informatisé de planification de chirurgie hépatique qui est utilisé à l’Hôpital de Strasbourg et s’est avéré significativement utile pour l’entraînement et la pratique chirurgicale dans ce centre hospitalier.
Modélisation physique
La modélisation de la nature déformable des biomatériaux est extrêmement compliquée au niveau informatique, ce qui fait de cette réalisation l’un des éléments les plus critiques pour permettre des performances en temps réel. C’est pour cette raison que, depuis 1995, nous nous penchons sur la définition de nouveaux algorithmes permettant une déformation réaliste des tissus mous, tout en maintenant les temps de calcul à un niveau raisonnable.
À des fins de réalisme, nous avons choisi de nous placer dans le cadre de la théorie de la mécanique des milieux continus (plus précisément, celle de l’élasticité) et de la méthode d’analyse par éléments finis. La théorie de l’élasticité a servi de base pour estimer la déformation des structures déformables depuis plus d’un siècle, en particulier dans le génie civil. En complément, comme méthode de référence servant à transformer un problème de mécanique en un problème mathématique, nous avons utilisé la méthode d’analyse par éléments finis. Toutefois, nous savions que ces approches pouvaient nécessiter des heures voire des jours de traitement informatique pour résoudre un problème donné. Notre contribution a été de proposer de nouveaux algorithmes permettant de calculer la déformation des tissus mous en quelques millisecondes.
Nous avons proposé deux approches complémentaires pour optimiser le calcul des déformations d’un matériau linéaire élastique sur la base de la méthode d’analyse par éléments finis.
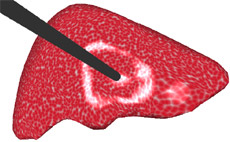
Déformation du foie obtenue à partir de la combinaison linéaire des déformations élémentaires précalculées.
La première approche exploite la linéarité du modèle pendant une étape de calcul préalable. En effet, une conséquence directe du modèle linéaire est que la déformation sous l’application de plusieurs forces est obtenue par l’addition des déformations produites par chaque force, indépendamment. Par conséquent, il est possible de calculer à un stade préliminaire un jeu de déformations obtenues à partir des forces élémentaires appliquées à chaque nœud et de conserver cette information. Pendant la simulation, il suffit alors de calculer une combinaison linéaire de ces déformations mémorisées pour en déduire les déformations réelles du modèle. Ceci permet de calculer la déformation d’un organe complet comme le foie en quelques millisecondes.
La limite principale de cette première approche tient au fait que la stratégie de calcul préalable suppose que la topologie du maillage du modèle reste la même pendant la simulation : ceci empêche évidemment la simulation de résection avec un scalpel ou des gestes de suture. En outre, cette méthode est également un procédé quasi statique car elle calcule directement la solution d’équilibre produite par l’application de l’instrument contre la surface du foie. Elle ne prend pas en compte la nature viscoélastique des tissus mous.
En raison de ces limites, nous avons proposé une deuxième approche introduisant des modèles déformables qui partagent un certain nombre de similitudes avec les modèles « masse – ressort » couramment utilisés dans le domaine de la synthèse d’images. L’avantage principal (et essentiel) de ces nouveaux modèles provient du fait qu’ils mettent réellement en œuvre une approximation discrète d’un comportement mécanique volumétrique et continu, ce qui n’est généralement pas le cas avec des modèles masse – ressort classiques. Cette deuxième approche demande plus de temps de calcul car elle nécessite l’intégration de l’équation différentielle du mouvement à chaque itération. Par conséquent, en fonction des performances de l’ordinateur et de la rigidité du matériau, il est nécessaire de limiter le nombre de nœuds du maillage afin de satisfaire aux contraintes de la mise en œuvre en temps réel (habituellement quelques milliers de nœuds sur un PC moderne).
C’est pour cette raison que nous avons introduit les modèles hybrides qui combinent les modèles pré-calculés et les modèles déformables. En limitant les régions sur lesquelles une résection avec un scalpel est possible, cela permet par conséquent d’inclure dans le simulateur des modèles déformables de grande taille. Dans le contexte de la chirurgie hépatique, nous avons décomposé notre modèle en huit régions, correspondant aux segments de Couinaud détectés, et nous avons limité les zones de résection à un certain nombre de zones en 3 D, situées à l’interface entre ces segments. Ces zones sont décrites par des modèles déformables alors que le reste du maillage est décrit par des modèles pré-calculés.
Restitution visuelle
Dans un projet en collaboration nommé AISIM, des outils spécifiques ont été développés par les chercheurs en synthèse d’images de l’équipe IMAGIS, pour produire une restitution réaliste du foie pendant une simulation chirurgicale. En particulier, la projection du reflet de la source de lumière circulaire utilisée dans la chirurgie laparoscopique renforce le réalisme et améliore la perception des déformations en 3 D du foie sous l’action des instruments. Une méthode originale de cartographie des textures a été introduite pour minimiser les distorsions de texture tout autour du modèle. De plus, la texture reproduit les marques créées par l’application de certains instruments tels qu’un scalpel électrique, augmentant encore le réalisme de la simulation.
 |
|
|
| Séquence d’une simulation de résection hépatique avec section de la veine porte. | Visionner une séquence vidéo de simulation – Durée : 1 min 06 s. |
Conclusions et perspectives
La mise en œuvre d’un simulateur chirurgical soulève de nombreuses difficultés liées à l’intégration de différentes technologies comprenant des interfaces utilisateur avancées, des éléments de mécanique simulés informatiquement, de robotique et d’infographie. En particulier, la restitution haptique et visuelle nécessite un taux de mise à jour élevé (plus de 1 000 Hz pour l’affichage haptique des matériaux informatiques), ce qui n’est pas compatible avecle coût de calcul informatique important requis pour modéliser les déformations des tissus mous. L’architecture actuelle de notre plate-forme de simulation se base sur un poste de travail graphique à processeurs multiples, dans lequel un processeur est consacré à l’extrapolation des forces envoyées aux dispositifs de restitution des forces.
La simulation des gestes chirurgicaux pose de nombreux problèmes scientifiques et technologiques importants. L’un des problèmes majeurs concerne le degré de connaissance du comportement physique des tissus humains. Actuellement, ces connaissances sont principalement qualitatives, il est donc de la plus haute importance pour de nombreuses applications biomédicales qu’un plus grand nombre d’études biomédicales soient menées dans un futur proche pour créer des modèles représentatifs et précis du corps humain.
Ce document est l’adaptation en français de l’article Hepatic Surgery Simulation paru dans Communications of the ACM Vol. 48, N° 2, février 2005 © ACM 2005.
Niveau de lecture
Aidez-nous à évaluer le niveau de lecture de ce document.
Votre choix a été pris en compte. Merci d'avoir estimé le niveau de ce document !

Hervé Delingette
Directeur de recherche Inria en simulation et analyse d'images médicales dans l'équipe ASCLEPIOS.

Nicholas Ayache
Directeur de recherche Inria, responsable de l'ancienne équipe ASCLEPIOS (désormais remplacée par EPIONE).