Vers la cellule virtuelle
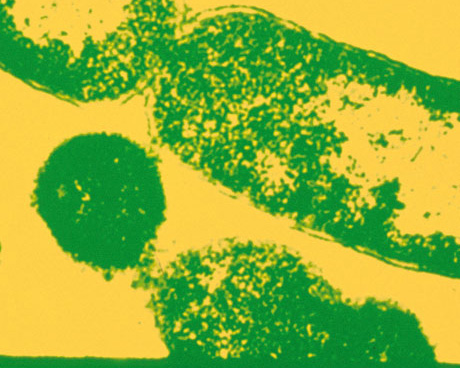
Bactéries Escherichia coli en division (© Institut Pasteur/Ryter A./Service photo).
Cette image colorisée permet de voir la bactérie intestinale Escherichia coli en cours de division. Avec un peu de sucre et de sels minéraux, elle grandit et se démultiplie jusqu’à plusieurs fois par heure !
Escherichia coli ou E. coli est une bactérie intestinale chez les mammifères, très commune chez l’homme. Découverte en 1885 par Theodor von Escherich (pédiatre et bactériologiste allemand), dans des selles de nourrissons, E. coli se nourrit dans le tube digestif de son hôte. Elle n’est généralement pas nocive, mais des souches pathogènes existent. Par exemple, elles peuvent entraîner des gastroentérites et des infections urinaires. Comme toutes les bactéries, E. coli est un organisme vivant unicellulaire. Elle est facile à cultiver en laboratoire et est devenue sans doute l’organisme vivant le mieux étudié. L’image colorisée montre des cellules d’E. coli en division. En présence d’un peu de sucre, de quelques sels minéraux et grâce à un réseau d’un millier de réactions métaboliques couplées, les cellules d’E. coligrandissent et se divisent jusqu’à plusieurs fois par heure ! Non seulement cette bactérie est un outil d’étude dans les laboratoires de biologie moléculaire, mais elle joue également un rôle important dans les biotechnologies, par exemple pour la production d’insuline et d’autres protéines ayant un intérêt médical.
La biologie moléculaire et la biochimie nous ont appris à voir les cellules des êtres vivants comme de microscopiques usines chimiques. Toutefois, cette image a ses limites, car les cellules ne sont pas construites comme des usines, par des ingénieurs, d’après des plans précis basés sur un cahier des charges. Les cellules vivantes ont été façonnées par l’évolution, sans plan préconçu, au cours d’un processus de bricolage sans fin. Mais il n’empêche que les outils de l’ingénieur, notamment les mathématiques et l’informatique, sont précieux pour mieux comprendre comment les fonctions principales de la cellule émergent de l’ensemble des réactions biochimiques entre ses éléments moléculaires. À partir d’une meilleure compréhension du fonctionnement de ce système extrêmement complexe, ces outils pourraient être d’une grande aide pour modifier les fonctions de la cellule, en vue de les adapter aux besoins de la recherche biomédicale et des biotechnologies.
L’être vivant à une cellule : la bactérie
Afin de mesurer la complexité de ces systèmes biochimiques que sont les cellules, regardons de plus près les bactéries, ces organismes unicellulaires aussi modestes qu’importants. Prenons l’exemple d’Escherichia coli (ou E. coli), une bactérie intestinale chez l’homme et d’autres mammifères. Il s’agit de l’un des organismes de choix des biologistes pour étudier les bases moléculaires de la vie. En effet, en présence d’un peu de sucre et de quelques sels minéraux, les cellules d’E. coli grandissent et se divisent jusqu’à plusieurs fois par heure. Leur croissance est assurée par un réseau d’un millier de réactions métaboliques couplées, qui absorbent les substances présentes dans le milieu et les transforment en énergie et en acides aminés. Les acides aminés sont les « briques de base » des protéines, qui elles-mêmes jouent plusieurs rôles importants dans la cellule. Elles en constituent non seulement la structure physique, comme la membrane qui sépare la cellule de son environnement, mais elles catalysent aussi, en tant qu’enzymes, les réactions métaboliques qui se produisent. Sans oublier qu’elles régulent la synthèse de ces mêmes protéines à partir des acides aminés, en suivant le programme génétique contenu dans l’ADN. Le tout forme un énorme réseau de réactions biochimiques, un système dans lequel se produisent des milliers de réactions en parallèle.
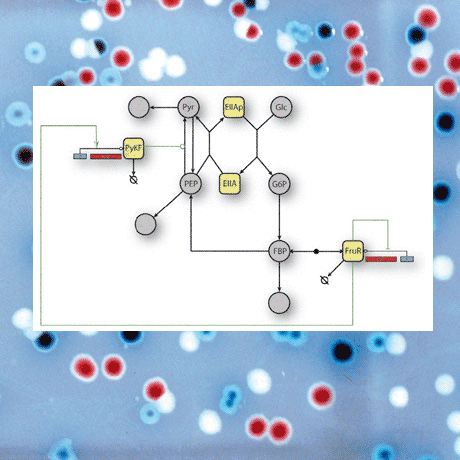
Médaillon : réseau de régulation chez la bactérie Escherichia coli (© Inria/Genostar)
Photo : colonies d’E. coli (© Institut Pasteur/Schwartz M.).
Lorsqu’un nouvel élément, comme du sucre par exemple, est introduit dans l’environnement d’une cellule, celle-ci réagit d’une certaine manière. On peut ainsi schématiser les « réactions biochimiques » qui sont à l’origine de ces comportements.
La figure montre un fragment du réseau de régulation de l’assimilation du glucose chez la bactérie E. coli. Ce schéma est la première étape dans la modélisation d’un système de réactions biochimiques. Après son entrée dans la cellule, le glucose (Glc) est dégradé par une chaîne de réactions métaboliques, produisant du pyruvate (Pyr). Chaque réaction est catalysée par une enzyme, comme PykF qui accélère la conversion de phospho-énol-pyruvate (PEP) en pyruvate. L’enzyme est produite à partir d’un gène dont l’expression est régulée par la protéine régulatrice FruR. Les réactions forment un réseau complexe, qui dans un deuxième temps est transformé en équations mathématiques. Le modèle permet de prédire la réponse du système à l’épuisement du glucose, comme la disparition de la protéine régulatrice EIIA, au profit de sa forme modifiée EIIAp. L’accumulation de EIIAp lève indirectement la répression des enzymes permettant la croissance de la cellule sur un sucre alternatif, le lactose.
Schématiser les réactions des cellules
Les livres de biochimie débordent de schémas qui représentent ce réseau, développés à un niveau de détail qui dépasse ce que nous pouvons faire ici. L’exemple de l’illustration présentée ci-dessus, qui schématise une petite partie de ce réseau responsable de l’assimilation du glucose, nous montre déjà qu’il n’est pas simple d’appréhender le déroulement des processus cellulaires. Est-ce que la concentration d’une enzyme va augmenter ou diminuer quand le glucose s’épuise ? Quand nous avons affaire à des systèmes aussi complexes où les boucles de rétroaction se multiplient et se croisent, il devient pratiquement impossible de prédire correctement la réponse de la cellule. L’intuition seule ne suffit plus.
L’ordinateur au secours du biologiste
L’alternative est de faire appel à l’ordinateur. Contrairement aux humains, un ordinateur n’est pas en difficulté quand il faut tenir compte d’un grand nombre de processus en parallèle. Cependant, un schéma comme celui présenté ci-contre ne lui suffit pas. Un ordinateur a besoin de connaître de façon précise et non ambiguë le sens de tous les symboles, de toutes les relations. La démarche de spécifier formellement ce que l’on sait du système s’appelle la « modélisation ». Elle débouche sur un modèle, souvent sous forme d’équations différentielles, que l’on peut notamment utiliser pour simuler les réactions biochimiques et ainsi prédire l’adaptation de la cellule à des changements dans son environnement. La modélisation aide le biologiste à formuler un processus complexe comme un système de réactions couplées. Chaque réaction et chaque espèce moléculaire ont un rôle précis dans la cellule, que l’on saisit en considérant le système dans son ensemble. Pour cette raison, l’approche qui combine expériences biologiques avec modèles mathématiques et simulations informatiques est appelée « biologie des systèmes ».
Il est important de souligner que la traduction de nos connaissances en un modèle mathématique n’a rien d’automatique. Le modélisateur décide ce qu’il est important d’inclure ou ce qu’on peut omettre, fixe le niveau de détail de la description, choisit entre différentes interprétations des données expérimentales… Il n’y a pas qu’un seul modèle, mais autant de modèles que de questions auxquelles le biologiste voudrait répondre. De ce point de vue, chaque modèle ressemble à une carte routière : la même carte ne peut pas servir pour se repérer dans le village qu’on visite ou pour se rendre d’un bout du pays à l’autre.
À chaque question son modèle

Colonie de bactéries Escherichia coli cultivées en boîte de Petri (© Inra/Nicolas B.)
Plusieurs modèles mathématiques du réseau responsable de l’assimilation de sucres chez les bactéries ont ainsi été développés par le passé. Un bon exemple est celui proposé par une équipe de chercheurs allemands, qui s’intéressent à la façon dont les bactéries croissent sur différents sucres, dans un ordre préférentiel. Par exemple, en présence de glucose et de lactose, E. coli va d’abord consommer le glucose, qui permet un taux de croissance plus élevé que le lactose. Une fois le glucose épuisé, les bactéries se mettent à consommer le lactose, en adaptant le fonctionnement de leur métabolisme. Mais comment l’épuisement du glucose est-il détecté par la cellule ? Et par quel mécanisme le pan du métabolisme responsable de l’assimilation de lactose est-il ensuite activé ? Les simulations numériques à l’aide du modèle ont mis en évidence le rôle clé d’une protéine régulatrice détectant l’épuisement du glucose. L’obtention d’un modèle qui reproduit aussi fidèlement la réponse de la cellule au niveau moléculaire, à la fois qualitativement et quantitativement, est un résultat important. Il se base sur un énorme travail de modélisation : les chercheurs allemands ont dû formuler plus de 60 équations et recenser des valeurs plausibles pour plus de 150 paramètres ! Une grande partie de ces paramètres ont dû être estimés à partir de nouvelles expériences, parce qu’ils n’avaient encore jamais été mesurés.
La simulation : une clé pour prédire
Cette calibration du modèle par rapport aux données expérimentales, nécessaire pour lui conférer une valeur prédictive, demande en général une grande quantité de données précises. Or, dans la plupart des cas, le modélisateur ne dispose pas de données de cette qualité. Il utilise alors parfois d’autres types de modèles, qui rendent l’analyse mathématique possible même sans informations quantitatives détaillées. Il peut ainsi avoir recours à des modèles simplifiés comme les réseaux booléens. Ces modèles traitent le système de réactions biochimiques comme un circuit électronique, où les réactions sont des composants réalisant des opérations logiques, et les éléments moléculaires produits par ces réactions sont les sorties des opérations, prenant des valeurs 0 ou 1 selon qu’ils sont absents ou présents. Il est clair que les prédictions ainsi obtenues sont plus faibles,mais si la précision quantitative n’est pas nécessaire, elles peuvent s’avérer bien utiles !
Mettre les cellules au travail
Un modèle peut aussi être traité non pas comme une description des bases moléculaires du fonctionnement de la cellule, mais comme un plan pour modifier ce fonctionnement. Les cellules atteindront-elles un taux de croissance plus élevé avec la même quantité de glucose si l’on change le réseau des réactions biochimiques ? Par exemple, en ajoutant une nouvelle réaction ou en diminuant l’effet d’une protéine régulatrice sur l’activité d’une enzyme ? Ce questionnement change le rôle du modèle. Il ne s’agit plus alors d’expliquer le déroulement des processus cellulaires, mais de tester des spécifications pour atteindre un objectif ayant un intérêt industriel ou médical. Le modèle ressemble alors plus à un plan d’architecte qu’à une carte routière.
L’utilisation des modèles pour mieux contrôler et transformer les processus cellulaires fait partie du domaine de la biotechnologie. Elle est à l’origine d’une nouvelle discipline, la « biologie synthétique ». Celle-ci cherche à concevoir par ordinateur des réseaux de réactions biochimiques, en faisant appel à une librairie de modules standardisés avec un fonctionnement certifié. Ces modules peuvent être de petits circuits de régulation, qui fonctionnent par exemple comme une bascule en réponse à un signal extérieur, mais également des chaînes de réactions métaboliques entières. Une étude récente, d’une équipe de chercheurs américains, a montré que la transplantation d’une voie métabolique d’un organisme à un autre est prometteuse. Les chercheurs ont intégré la capacité d’une plante à produire le précurseur de l’artémisinine, la substance active d’un médicament contre la malaria, dans la levure. Ceci permet d’augmenter l’efficacité de la production d’artémisinine et pourrait, à terme, réduire les coûts du médicament.
La conception assistée par ordinateur des réseaux synthétiques n’en est aujourd’hui qu’à ses débuts. Est-ce que les cellules vivantes pourront être traitées comme des voitures, des avions ou des ordinateurs ? Il se peut qu’au contraire, la biologie synthétique remettra en cause les principes classiques de l’ingénierie.
Livres
- Rechenmann F., Jong (de) H., « Le vivant en équations », in La Recherche, n° 383, 2005.
- Ropers D., Jong (de) H., Geiselmann J., « Modélisation de la réponse au stress nutritionnel de la bactérie Escherichia coli », in Biofutur, n° 275, 2007. Voir aussi les autres articles dans ce numéro spécial, notamment ceux d’A. Siegel et de J.-P. Mazat.
Sites web
Cet article est paru dans la revue DocSciences n°8 Le numérique et les sciences du vivant, éditée par le CRDP de l’Académie de Versailles en partenariat avec l’Inria.
Niveau de lecture
Aidez-nous à évaluer le niveau de lecture de ce document.
Votre choix a été pris en compte. Merci d'avoir estimé le niveau de ce document !

Hidde de Jong